発表のポイント
・タンパク質の液-液相分離を制御するペプチド設計法を考案
・神経変性疾患関連タンパク質FUSの液-液相分離や固体状の凝集体形成の制御に成功
概要
認知症やアルツハイマー病などの神経変性疾患には、液-液相分離する「相分離タンパク質」の関与が明らかとなってきました。液-液相分離とは、タンパク質が低い濃度で分散している液相中に、タンパク質の密集した液相が形成される現象です。タンパク質が一時的に密集することで、高効率な化学反応が可能となりますが、同時に、疾患の原因となる不溶性の凝集体が形成されるリスクがあります。東北大学多元物質科学研究所の鎌形清人准教授、東北大学薬学研究科の川畑伊知郎准教授、福永浩司教授、富山大学学術研究部薬学・和漢系の池田恵介准教授、および産業技術総合研究所人工知能研究センターの亀田倫史主任研究員らの研究グループは、相分離タンパク質を制御するペプチドの効率的な探索法として、液-液相分離を制御できるアミノ酸の探索を行い、効果の出たアミノ酸を含むペプチドを設計する方法を考案しました。この方法により、神経変性疾患に関与するタンパク質FUSの液-液相分離や固体状の凝集体形成の制御にも成功しました。今後、疾患に関与する相分離タンパク質を標的とした創薬への応用が期待されます。
本研究成果は、2021年3月23日(英国夏時間)に英国科学誌 Scientific Reports(オンライン版)に掲載されました。また、本研究は、科学研究費助成事業、および産総研-東北大マッチング事業の支援を受けて、実施されました。
プレスリリース本文(PDF)
研究背景
認知症やアルツハイマー病などの神経変性疾患には、液-液相分離する「相分離タンパク質」の関与が近年明らかとなってきました。液-液相分離とは、タンパク質が低い濃度で分散している液相中に、タンパク質が密集した液相を形成する現象です。タンパク質が一時的に密集することで、高効率な化学反応が可能となりますが、同時に、疾患の原因となる不溶性の凝集体が形成するリスクがあります。相分離タンパク質の創薬には、相分離タンパク質に結合し、液-液相分離や固体状の凝集体形成を制御できる医薬品候補分子の設計が必要となります。医薬品候補のペプチドは、相分離タンパク質にその形を変えて結合できるだけでなく、20種類の性質の異なるアミノ酸を並べることで、特異的な結合が期待できます。ところが、膨大な数のペプチド候補から制御できるものを見つけることは難しいとされてきました。
研究の成果
研究グループは、相分離タンパク質を制御するペプチドの効率的な探索法として、液-液相分離を制御できるアミノ酸の探索を行い、効果の出たアミノ酸を含むペプチドを設計する方法を考案しました。続いて、神経変性疾患に関与するタンパク質FUSを対象として、考案した方法の検証を行いました。試験管内で液-液相分離したFUSに対して、19種類のアミノ酸(システインを除く)を添加したところ、アルギニンとチロシンがFUSの液-液相分離を抑制することが分かりました。分子動力学シミュレーションから、アルギニンとチロシンは、液-液相分離したFUS分子間の結合(カチオン-π相互作用と静電相互作用)を阻害し、液-液相分離を抑制することが明らかとなりました(図A)。さらに、アルギニンを連結したペプチド(ポリアルギニン)を添加したところ、FUSの液-液相分離が促進されることが明らかとなりました。これは、ポリアルギニンが複数のFUS分子に結合し、液-液相分離を促進するためと考えられます(図B)。さらに、神経細胞を用いた実験においても、同様に、アルギニンとポリアルギニンによるFUS会合体の制御が見られました。続いて、アルギニンとポリアルギニンがFUSの固体状の凝集体形成に与える影響を調べたところ、アルギニンは抑制効果を示したのに対し、ポリアルギニンは促進効果を示すことが分かりました。これは、液-液相分離(反応の中間体)の制御が、固体状の凝集体形成の制御を可能にすることを表しています(図C)。以上より、相分離タンパク質の制御を可能とする、実験駆動型のペプチド設計法を提案しました。今後、様々な疾患に関与する相分離タンパク質を標的とした創薬への応用が期待されます。
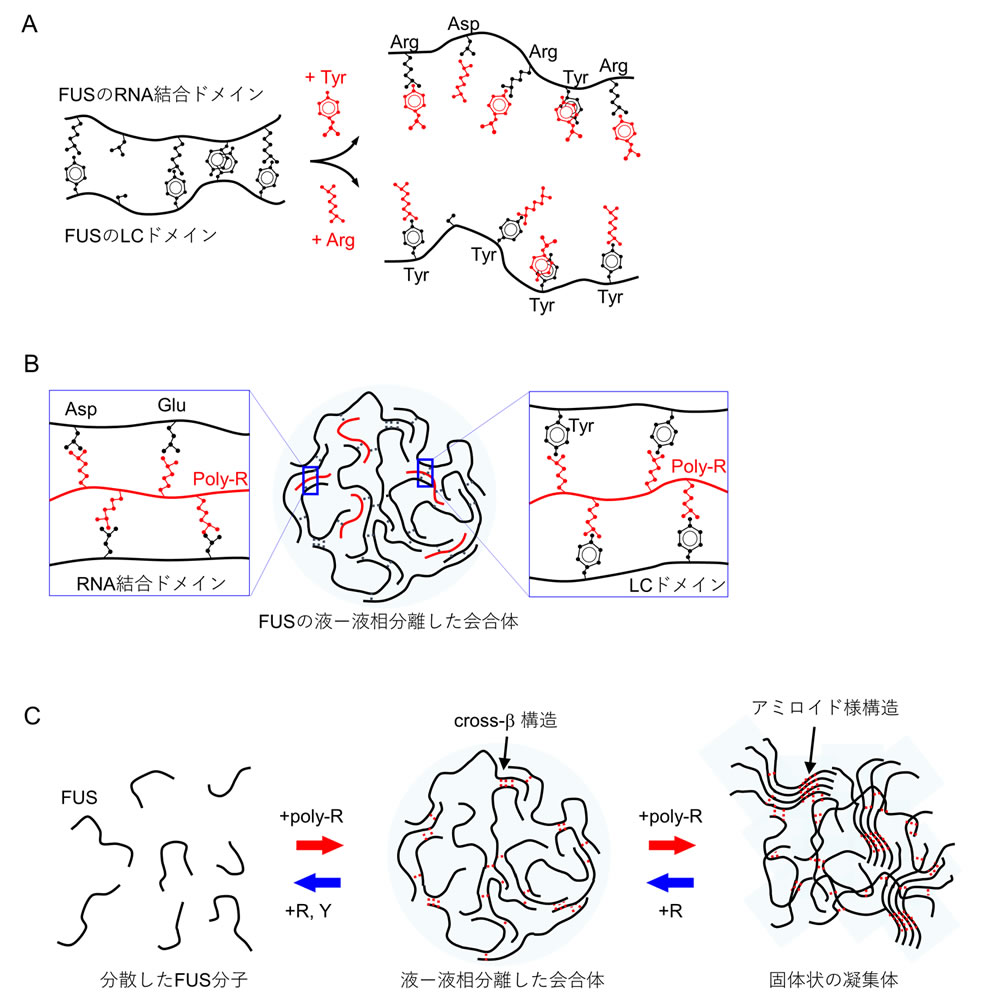
A)アルギニンとチロシンによるFUSの液-液相分離の抑制。FUSのLCドメインとRNA結合ドメインとの結合により、液-液相分離した会合体が形成されます(左図)。アルギニン(Arg)とチロシン(Tyr)は、FUSのLCドメインとRNA結合ドメインとの結合を阻害することで、FUSの液-液相分離を抑制します(右図)。
B)ポリアルギニン(poly-R)は、FUSのLCドメインやRNA結合ドメインに結合し、FUSの液-液相分離を促進します。
C)添加剤によるFUSの相分離の制御。RとYは、それぞれアルギニンとチロシンを表している。
原著論文の図より転載しました。
論文情報:
“Characterization of design grammar of peptides for regulating liquid droplets and aggregates of FUS”
Scientific Reports
Kiyoto Kamagata1,2,3*, Rika Chiba1,2, Ichiro Kawahata4, Nanako Iwaki1,3, Saori Kanbayashi1, Kana Maeda1,3, Hiroto Takahashi1, Atsushi Hirano5, Koji Fukunaga4, Keisuke Ikeda6, and Tomoshi Kameda7
1.東北大学多元物質科学研究所, 2.東北大学大学院生命科学研究科, 3.東北大学大学院理学研究科化学専攻, 4.東北大学薬学研究科, 5.産業技術総合研究所ナノ材料研究部門, 6.富山大学学術研究部薬学・和漢系, 7.産業技術総合研究所 人工知能研究センター
DOI:10.1038/s41598-021-86098-1
関連リンク:
東北大学ウェブサイト
生命分子ダイナミクス研究分野(髙橋聡研究室)
問い合わせ先
東北大学多元物質科学研究所
准教授 鎌形 清人(かまがた きよと)
電話: 022-217-5843
E-mail:kiyoto.kamagata.e8*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学多元物質科学研究所 広報情報室
E-mail:press.tagen*grp.tohoku.ac.jp(*を@に置き換えてください)