私達が目にするほとんどのガラスの主成分はSiO2である。
SiO2の他にB2O3 ,
P2O5等が単独でガラスになる。しかし、化学的に熱的にも一番安定なものはSiO2であるため、特殊な物*を除いて、ガラスの主成分はSiO2と言うことができる。
SiO2は岩石の主要成分であり、そのクラーク数はOが49.5 ,
Siが25.8である。したがってガラスの資源は無尽蔵であるといってよい。
ガラスはSiO2に他のものを混合し加熱溶融して作る。ガラスの成分とそれらのガラスの性質に対する影響を次に示す。
ケイ酸 SiO2
ガラスの網目構造を作る。軟化温度が高く、熱膨張係数が小さい。化学的に安定である。
ホウ酸 B2O3
ガラスの網目構造を作る。熱膨張係数や化学耐久性に変化を与えずに軟化温度を下げる。分相しやすい。
アルミナ Al2O3
結晶化を抑える。軟化温度を上げる。
酸化鉛 PbO
屈折率が大きい。還元ふん囲気ではPbになる。金属との濡れを良くする。
酸化ナトリウム Na2O
軟化温度を下げる。熱膨張係数を大きくする。化学耐久性を減少させる。
酸化カリウム K2O
Na2Oと同じ効果。
Na+より大きいので移動せず、化学耐久性はNa2Oより大きい。光沢を与える。
酸化カルシウム CaO
アルカリの移動を止めるためアルカリガラスの化学耐久性を増す。
以上のほか、MgO,
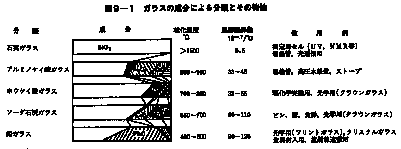
BaOなどがある。これらがどのような割合で混合されるかによりガラスの性質が決まる。ガラスの成分による分類とその特性を表9-1に示す。理化学実験に用いられるガラスは主に石英ガラスとホウケイ酸ガラスである。
*たとえば、ナトリウム放電ランプ用ガラスの主成分はB2O3
- Al2O3-BaOでSiO2を含まない。

石英ガラスには(1)水晶を酸水素炎で溶融したもの、(2)水晶を電気溶融したもの、(3)SiCl4を酸水素炎中で反応させたもの等がある。OH基による赤外部の吸収の少ないのは(2)法によるもので、紫外部の吸収の少ないのは(3)法によるものである。(3)法による合成石英を真空中で溶融する等によりOHを少なくしたものもある。理化学実験用のホウケイ酸ガラスの組成例を表9-2に示す。
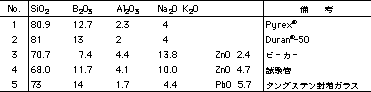
1,2のガラスは熱膨張係数が32×10-7/℃でアルカリ溶出度が小さい。3,4は1,2に比べ熱膨張係数とアルカリ溶出度が大きい。5はPbOを入れ金属との濡れを良くしたものである。
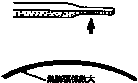
石英ガラス(熱膨張係数5.6×10-7/℃)とPyrexィ(熱膨張係数32×10-7/℃)のように熱膨張係数の異なるガラスをつなぐ場合、熱膨張係数の少しずつ異なるガラス(中間ガラス)を何種か間にはさんで熱膨張係数の差によるひずみを緩和させる。ガラスの熱膨張係数がわからない場合は次のようにして調べる。接ぎ合わせたいガラスを重ね合わせ、加熱し溶着させて引き伸ばす。冷却後、二つのガラス熱膨張係数が等しければ、補足引き伸ばされた部分は直線となり、等しくなければ、熱膨張係数の大きいガラスを内側にして弧を描いて曲がる。曲がり方の小さいときは二つのガラスを直接接合できるが、曲がり方の大きいときは間に中間ガラスを入れる必要がある。