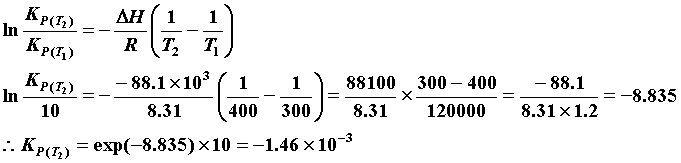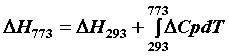 で、計算できる。単位に気をつけること。kJだったり、Jだったり。
で、計算できる。単位に気をつけること。kJだったり、Jだったり。小テスト&基本調査 平成
10年6月16日
1.
次のそれぞれの溶液に、固体のAgClを十分な量添加し、溶解平衡に達した。理想溶液として、溶液中に存在する25℃におけるAg+イオン濃度をそれぞれの場合について、計算せよ。なお、AgClの溶解度積 [Ag+] [Cl-] = 1.8 x 10-10 mol2/l2 at 25 ℃。(a) NaCl: 1 x 10-3 mol/l
溶液 (b) pH = 5 の溶液<考え方>
(a)は、Cl-イオン濃度が1 x 10-3 mol/lとして、(b)は、溶液中にCl-イオンが予めがないので、[Ag+]=[Cl-]として解く。
2. 20
℃, 1 atmにおけるC(グラファイト), H2, CH4の燃焼熱ΔHは、それぞれ-394.13, -285.95, -891.10 kJ/mol
である。0℃から600℃の間の定圧モル比熱CpはC(
グラファイト): Cp = 4.60 + 0.02008 T ? 0.000005 T2H2: Cp = 27.20 + 0.0038 T
CH4: Cp = 22.34 + 0.0481 T
このとき、
500℃, 1 atmでのメタンの生成熱を求めよ。<ヒント>
C(グラファイト), H2, CH4の燃焼反応は、それぞれ次のように書ける。C + O2 ? CO2 + ΔH1
H2 + 1/2 O2 ? H2O + ΔH2
CH4 + 2O2 ? CO2 + 2 H2O + ΔH3
従って、メタンの生成反応は、
C + 2 H2
→ CH4 + ΔHf で(ここで、ΔHfは生成熱)生成エンタルピー変化は
Δ
また、定圧モル比熱変化
ΔCpは、定義よりΔ
だから、 Δ
Cp = CpCH4 - CpC - 2 x CpH2 = ??すると、500℃のときのΔHfは、ΔHf =ΔH0 +∫ΔCp dT、
つまり、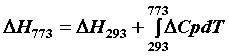 で、計算できる。単位に気をつけること。kJだったり、Jだったり。
で、計算できる。単位に気をつけること。kJだったり、Jだったり。
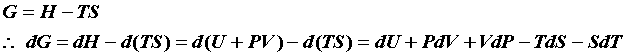 3.
3.
可逆変化で仕事が体積変化だけによる場合で![]() となり、圧力一定のとき、
となり、圧力一定のとき、![]() あるいは、
あるいは、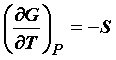 となる。つまり、定圧における
となる。つまり、定圧における
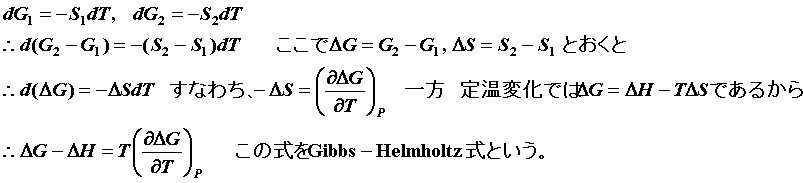
●![]() という関係式は、化学ポテンシャルの関係式から次のように導出できる。
という関係式は、化学ポテンシャルの関係式から次のように導出できる。

(a) 2CO + O2
? 2CO2 の反応の25℃における平衡定数Kpを計算せよ。ただし、COとCO2のそれぞれの25℃の標準生成自由エネルギー(b) ![]() を変形することにより、ファントホッフ定圧平衡式
を変形することにより、ファントホッフ定圧平衡式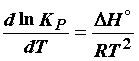 を導き出せ。
を導き出せ。
<ヒント>![]() の両辺をTで偏微分し、Gibbs-Helmholts式を代入する。
の両辺をTで偏微分し、Gibbs-Helmholts式を代入する。
(c)
ファントホッフの定圧平衡式は定積分すると、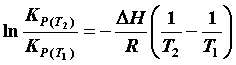 となる。ここで、
となる。ここで、単位に気を付けること。
(解答例)
小テスト&基本調査 平成
10年6月16日
1.
次のそれぞれの溶液に、固体のAgClを十分な量添加し、溶解平衡に達した。理想溶液として、溶液中に存在する25℃におけるAg+イオン濃度をそれぞれの場合について、計算せよ。なお、AgClの溶解度積 [Ag+] [Cl-] = 1.8 x 10-10 mol2/l2 at 25 ℃。(a) NaCl: 1 x 10-3 mol/l
溶液 (b) pH = 5 の溶液<考え方>
(a)は、Cl-イオン濃度が1 x 10-3 mol/lとして、(b)は、溶液中にCl-イオンが予めがないので、[Ag+]=[Cl-]として解く。
2. 20
℃, 1 atmにおけるC(グラファイト), H2, CH4の燃焼熱ΔHは、それぞれ-394.13, -285.95, -891.10 kJ/mol
である。0℃から600℃の間の定圧モル比熱CpはC(
グラファイト): Cp = 4.60 + 0.02008 T ? 0.000005 T2H2: Cp = 27.20 + 0.0038 T
CH4: Cp = 22.34 + 0.0481 T
このとき、
500℃, 1 atmでのメタンの生成熱を求めよ。<解答例>
C(グラファイト), H2, CH4の燃焼反応は、それぞれ次のように書ける。C + O2 ? CO2 + ΔH1
H2 + 1/2 O2 ? H2O + ΔH2
CH4 + 2O2 ? CO2 + 2 H2O + ΔH3
従って、メタンの生成反応は、
C + 2 H2
→ CH4 + ΔHf で(ここで、ΔHfは生成熱)生成エンタルピー変化は
Δ
= -74.93 kJ/mol
(これは20℃のとき)また、定圧モル比熱変化
ΔCpは、定義よりΔ
だから、 Δ
Cp = CpCH4 - CpC - 2 x CpH2 == 22.34 + 0.0481 T - {4.60 + 0.02008 T ? 0.000005 T2 + 2 x (27.20 +
0.0038 T)}
= -36.66 + 0.02042 T + 0.000005 T2
すると、
500℃のときのΔHfは、ΔHf =ΔH0 +∫ΔCp dT、つまり、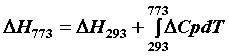 で、計算できる。単位に気をつけること。
で、計算できる。単位に気をつけること。
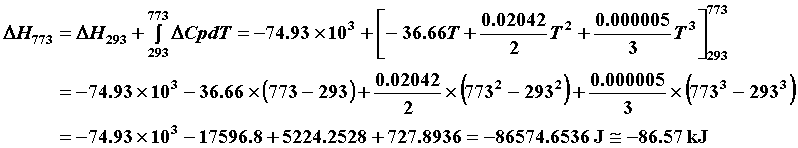
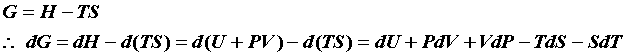 3.
3.
可逆変化で仕事が体積変化だけによる場合で![]() となり、圧力一定のとき、
となり、圧力一定のとき、![]() あるいは、
あるいは、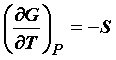 となる。つまり、定圧における
となる。つまり、定圧における
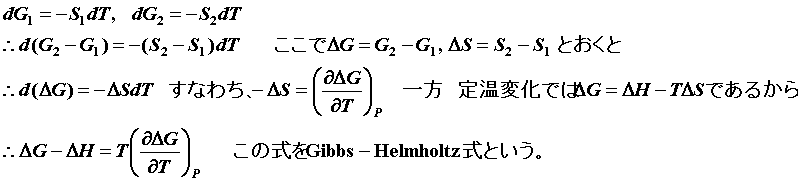
●![]() という関係式は、化学ポテンシャルの関係式から次のように導出できる。
という関係式は、化学ポテンシャルの関係式から次のように導出できる。

(a) 2CO + O2
? 2CO2 の反応の25℃における平衡定数Kpを計算せよ。ただし、COとCO2のそれぞれの25℃の標準生成自由エネルギー<解答例>
Δ
G = 2xΔG CO2 - 2xΔG CO=2 x (-394.4) - 2 x (-137.2) = -514= - RT ln KpKp = exp (-ΔG / RT) = exp (514000 / 8.31 / 298) = 1.39 x 1090
(b) ![]() を変形することにより、ファントホッフ定圧平衡式
を変形することにより、ファントホッフ定圧平衡式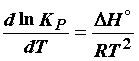 を導き出せ。
を導き出せ。
<ヒント>![]() の両辺をTで偏微分し、Gibbs-Helmholts式を代入する。
の両辺をTで偏微分し、Gibbs-Helmholts式を代入する。
<解答例>

(c)
ファントホッフの定圧平衡式は定積分すると、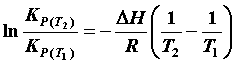 となる。ここで、
となる。ここで、単位に気を付けること。
<解答例>